Terapia Cluj donează spitalelor din România 48.500 de cutii de Favipiravir
Ministerul Sănătății anunță că Guvernul a aprobat donația, care urmează să fie repartizată către unitățile sanitare care tratează bolnavi de COVID-19.
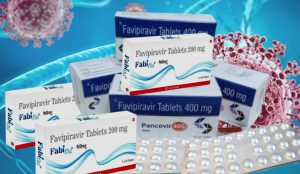 Guvernul României a aprobat joi, 28 octombrie 2021, un proiect de Hotărâre prin care statul român acceptă, prin Ministerul Sănătății, o donaţie de medicamente constând în 48.500 de cutii de Favipiravirum, din partea societății Terapia SA, și darea în administrare a acestora, în scopul repartizării către unitățile sanitare care tratează bolnavi de COVID-19, anunță Ministerul Sănătății, printr-un comunicat.
Guvernul României a aprobat joi, 28 octombrie 2021, un proiect de Hotărâre prin care statul român acceptă, prin Ministerul Sănătății, o donaţie de medicamente constând în 48.500 de cutii de Favipiravirum, din partea societății Terapia SA, și darea în administrare a acestora, în scopul repartizării către unitățile sanitare care tratează bolnavi de COVID-19, anunță Ministerul Sănătății, printr-un comunicat.
,,Apreciem gestul societății Terapia S.A care vine în sprijinul pacienților româniˮ a declarat Cseke Attila, ministrul interimar al Sănătății, menționând că medicamentele vor fi repartizate gratuit, unităților medicale care tratează pacienți COVID-19.
MS reamintșete că, luna aceasta, a reglementat eliberarea medicamentului Favipiravir în ambulatoriu, prin farmaciile cu circuit închis din cadrul spitalelor, cu prescripție medicală, conform recomandărilor specialiștilor din Comisia de specialitate de boli infecțioase.
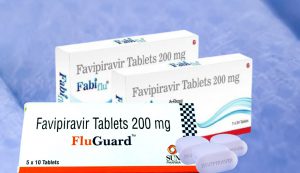
Produsul este importat din India și comercializat sub denumirea de FluGuard. Inițial a fost dezvoltat pentru gripă, dar ulterior s-a folosit și împotriva Ebola și COVID.
 Conform Protocolului Național de tratament al bolnavilor infectați cu virusul SARS-Cov-2, medicamentul Favipiravir reduce febra și este recomandat să fie administrat în formele ușoare și medii de infecție cu noul corornavirus doar în prima săptămână de boală, când pacientul este în faza presimptomatică.
Conform Protocolului Național de tratament al bolnavilor infectați cu virusul SARS-Cov-2, medicamentul Favipiravir reduce febra și este recomandat să fie administrat în formele ușoare și medii de infecție cu noul corornavirus doar în prima săptămână de boală, când pacientul este în faza presimptomatică.
Acuzată că nu a admis eliberarea medicamentului prin farmaciile cu circuit deschis, dr. Ioana Mihăilă, fostul ministru al Sănătății, scrie pe contul său de socializare că „toate deciziile pe care le-am luat în legătură cu acest medicament le-am luat strict prin decizia specialiștilor” și subliniază că „Favipiravir este un medicament care se utilizează la scară mică, un medicament cu potențial teratogen (malformații). Favipiravir prezintă risc de creștere a enzimelor hepatice (AST, ALT, GGT) și de afectare hepatică/apariție a leziunilor hepatice induse medicamentos, precum și risc de hiperuricemie. Este absolut necesar controlul strict al eliberării, sub stricta supraveghere a medicilor”, de aceea „este absolut necesar controlul strict al eliberării, sub stricta supraveghere a medicilor”.
 Dragoș Damian, directorul executiv Terapia, spune că la Cluj ar putea produce 100.000 de cutii de Favipiravir pe lună, dar deși a cerut în urmă cu 6 luni să producă în România acest medicament, Agenția Națională a Medicamentului și Dispozitivelor Medicale din România că nu i-a răspuns, iar fără avizul ANMDMR nu poate face nimic. El a subliniat că în absența acestui medicament din farmacii, pericolul este că, acum, în România s-a dezvoltat o piață neagră de medicamente antivirale.
Dragoș Damian, directorul executiv Terapia, spune că la Cluj ar putea produce 100.000 de cutii de Favipiravir pe lună, dar deși a cerut în urmă cu 6 luni să producă în România acest medicament, Agenția Națională a Medicamentului și Dispozitivelor Medicale din România că nu i-a răspuns, iar fără avizul ANMDMR nu poate face nimic. El a subliniat că în absența acestui medicament din farmacii, pericolul este că, acum, în România s-a dezvoltat o piață neagră de medicamente antivirale.
Hindustan Times a scris însă, în data de 7 iunie, că India (țară în care se produce medicamentul) a renunțat la folosirea favipiravir în protocolul de tratare a pacienților cu COVID.
Agenția Națională a Medicamentului atrage atenția în „fișa informativă pentru pacienți cu privire la medicamentul FluGuard 200 mg comprimate filmate (favipiravir)” asupra riscurilor de „teratogenicitate” și de „afectare hepatică și risc de creștere a acidului uric din sânge (hiperuricemie)”.














 Buzau: www.newmedical.ro
Buzau: www.newmedical.ro

